当科の研究とは
当科では、その特徴である症例数を生かした臨床に基づく研究を多数行っており、世界的に意義のある研究結果を常に出し続けています。そのため、研究に対する身近な環境が出来上がっており、医局員の日常臨床にも研究に対する向上心が染み渡っていることが、患者さんに還元できるアカデミックな医療を行う姿勢に結びついていると考えています。
、世界随一の心筋病理の研究ができることは間違いありません。基礎研究の分野においても、臨床に直結していることが、当科の研究の特徴の一つと言えるでしょう。
大学院、臨床大学院制度
大学院では、研究に共通する基本的な能力(研究の進め方や論文の書き方)をきちんと学び、それに基づき研究を行うための十分な時間と環境が準備されています。大学院で得た能力・考え方というのは、臨床だけでは学べない、先生方の一生の宝になることでしょう。 また当科では、後期研修を行いつつ大学院へ進むことができる臨床大学院制度も実施しています。後期研修の2年で循環器診療の基本を学び、その臨床能力を維持するため最低限の臨床を行いつつも、なるべく研究に専念できる時間を持てる環境を実現しています。臨床大学院制度により、まだまだ成長途中である臨床能力を維持できるため、大学院卒業後臨床現場への復帰がよりスムーズになるものと思われます。
大学院に入学する時期については、後期研修の初め2年は、その後の医療人としての基礎を形成するために臨床に従事することを推奨していますが、それ以降は個々に相談することが可能です。
研究分野: 指導医
臨床
- 不整脈
- 心房細動のアブレーション後再発予測因子の検討
- 心房のリモデリングと心房細動アブレーションの有効性に関する検討
- 重症低心機能症例に合併した心房細動に対するアブレーションの有用性に関する検討
- 心房細動アブレーション後の待機時間と術後再発に関する検討
- 心房細動に対するempiricな追加焼灼の有効性に関する検討
- 持続性心房細動に対するアブレーションの治療効果予測における心内電位解析の検討
- 心房細動アブレーションにおけるdurable lesion達成の方法に関する検討
- 希少疾患に合併した心房細動に対するカテーテルアブレーションの有用性に関する検討
- 心耳の形態と心房細動の病態に関する検討
- 小児例、先天性心疾患例に対するカテーテルアブレーションに関する検討(循環器小児科と共同)
- 心室頻拍に対するアブレーションの有効性に関する検討
- 多形性心室頻拍、心室細動の誘引となる心室期外収縮に対するアブレーションの有効性に関する検討
- 遠隔モニタリングを用いた不整脈イベントに関する検討
- 遠隔モニタリングを用いたICDの作動予測因子の検討
- テーラーメードな心臓再同期療法の検討
- ICD植え込み後症例におけるhigh DFTの予測因子に関する検討
- 小児例、先天性心疾患例に対するに植え込み型デバイス治療関する検討(循環器小児科と共同)
- 多施設共同大規模臨床研究(ASSERT, MADIT-RIT, HomeCARE, DetectICIなど)
- リード抜去治療(レーザーシステム、メカニカルシース)に関する検討
-
心不全
心不全は高血圧、虚血性心疾患、弁膜症、心筋症、不整脈などの基礎心疾患を有する病態の末期像であります。そのため、心不全といっても病態は複雑であり、その治療も単一化されたものではありません。さらに、心臓のみならず全身から病態を考え、治療していく必要があります。このミステリアスな領域を日夜、エネルギッシュに、多方向からの視点、マスから個と多彩なアプローチで取り組んでいます。
- 心不全コホート
- 心筋症
- 心不全と不整脈
- 急性心不全
- 肺高血圧
- 薬物治療
- 心臓リハビリテーションと心身医学
当院循環器内科では、2000年代より関連病院と多施設共同研究を行い、日本人における心不全患者の臨床背景と治療実態についてコホート研究を行ってきました。2001~2002年の心不全入院患者を対象としたHIJ-HF I、2013~14年の心不全入院患者を対象としたHIJ-HF II、そして現在HIJ-HF IIIの前向き登録研究が進行しています。そのなかで日本人の心不全患者では臨床背景が欧米と異なることを明らかにしてきました。また、高齢化社会のなかで心不全患者は増加の一途です。日本人の慢性心不全患者の予後および生活の質の改善を目標とし、どのような介入点が必要なのか、またどのような治療が相応しいのか、在宅医療とどうリンクさせていくのか、費用対効果も含めて多方向から解析しています。特発性拡張型心筋症:
特発性拡張型心筋症は、原因不明の心筋疾患とされ、多くの研究が行われていますが、不良の転帰をとる症例も少なくないのが現状です。当院は心臓移植登録施設でもあることから、家族性も含めた長期にわたって通院治療されている症例も多く、心不全発症に結びつく病態と予後との関連性を解明する上で豊富な臨床データを有しています。一症例一症例の臨床経過を踏まえたデータ解析研究のほか、最近では遺伝子解析も含めた基礎データをもとにテーラーメード治療を確立できるよう研究を進めています。肥大型心筋症:
当院循環器内科には長い歴史があり、年月をかけて600例前後の肥大型心筋症の症例経験が蓄積されています。その診療情報から臨床研究を行うことで、学会発表および国際誌への論文発表を行っています。多くの症例の後ろ向きコホート研究から、リスクの層別化など詳細な疫学データを論文化することで、心筋症の臨床研究に世界的な貢献をすることが求められています。また治療薬および手技の効果を判定するなどの、小規模な介入研究を通して、肥大型心筋症の病態を解明していくことを目指しています。また今後は、多施設共同の前向き研究への参加も検討しており、ますます発展が期待できる領域と考えています。心サルコイドーシス:
心サルコイドーシスは肉芽腫(類上皮細胞肉芽腫)性疾患で心病変の合併は20-30%とされ、特定疾患に指定されている心筋症の一つです。心サルコイドーシスは日本人に多く、2012年にPET検査が本邦で保険償還されてから、その病態の解明が進み、疫学や診断、活動性評価など多くの報告が日本から出ています。一方で、その原因は未だ不明で、診断(病理診断率の低さ、画像検査による診断精度など)、治療(免疫抑制剤併用やデバイス適応など)も確立されておらず、さらなる検討が必要な領域であります。当院ではこれまで100例を超える心サルコイドーシスの症例を経験し、画像診断や電気生理、病理グループと共同で最新の診療方法と治療戦略の確立を目指して研究をしています。不整脈源性右室心筋症:
当院の長い歴史で特筆すべきは、心筋生検法を日本で最初に開発し、その臨床応用に大きく貢献してきたことです。このため、心筋症の診断も古くから高い精度を持って行われてきました。不整脈源性右室心筋症について、単施設では世界有数の症例と経験を有し、現在100例を超すコホート研究について解析を進めています。不整脈治療のみならず、突然死の余地、心不全進行の機序など遺伝子解析から臨床まで幅広い視野から、本疾患の解明と治療戦略の開発に取り組んでいます。心不全患者の死因として多い心臓突然死の予防治療(植込み型除細動器、カテーテルアブレーション、抗不整脈薬アミオダロン使用など)にも古くから取り組んでおり、その実績は日本でもトップクラスです。心電学的検討を含めた不整脈リスク因子の研究を主とし、心不全における不整脈の成因・病態・治療に関する研究を行っています。臨床研究では心不全における不整脈基質の判断とリスク層別化から、突然死予防に向けての治療戦略の開発を目指しています。また、不全心の心臓電気現象および機械的現象をリンクされる新しいモダリティの開発も行っています。当院は循環器救急診療に力を入れており、10病床あるCCU(Coronary Care Unit)で、主に急性冠症候群、急性心不全のなど循環器緊急疾患の治療を多く行っています。なかでも急性心不全患者は、高齢化や冠疾患に対する治療の進歩から、近年非常にその数が増えてきており、疫学的にもその臨床研究の必要性が高まってきています。当院にも多くの急性心不全患者が入院しますので、その診療情報から臨床研究を行い、学会発表および国際誌への論文発表を行っています。多施設共同研究、単施設からの詳細なコホート研究、小規模な介入研究などを行うことで、急性心不全の病態に迫り、論文として発表していくことを目指しています。肺高血圧症はかつて非常に予後不良な疾患でしたが、近年の薬物治療の進歩や新たな治療法の開発により、その治療成績は目覚ましい進歩を遂げています。また、それをリードしているのは日本発のエビデンスであり、本邦が世界をリードしている数少ない領域でもあります。当施設の症例は特発性肺動脈性肺高血圧のみではなく、先天性心疾患、膠原病や肝疾患による続発性肺高血圧症や重症心不全や呼吸器疾患に合併した肺高血圧までvarietyに富んでいるのが特徴です。重症例も多く、エポプロステノール持続静注やCTEPHに対する経皮的カテーテル治療(BPA)も積極的に行っています。このような知見をもとに国内外の学会や論文等での情報発信を行っており、さらなる肺高血圧症診療の進歩に寄与することを目標としています。非薬物治療が大きく進歩してきた循環器領域において、薬物治療は基本であり、まだ解明されていない点が多々あります。当教室では古くはジゴキシン、キニジンからアミオダロン、ニフェカラントという日本における抗不整脈薬の臨床開発の先頭を切ってきました。この背景には薬物血中濃度測定やモニタリングをいち早く導入し、科学的な薬物治療法の確立を目指してきたことがあります。心不全の薬物治療を大きなコホート研究から考えるベクトルと、循環器薬の病態時における薬物動態学的・薬力学的の変化、個人内の薬物血中濃度-効果関係モデル(PK-PDモデル)の作成、人種間による薬物代謝酵素、薬物感受性の相違およびその機序について検討し、個別化治療へ展開するというベクトルを持って研究しています。薬物療法と非薬物療法の進歩に伴い心不全治療は大きく変わってきました。一方で慢性心不全患者に併存する抑うつや不安といった精神的問題はそれ自身が予後悪化因子として認識されているものの依然として臨床医にとって大きな壁になっています。慢性心不全は全身病であり、包括的リハビリテーションの介入により生活の質(QOL)を向上させること、多職種による介入が有効であることは近年の多くの臨床試験から示されています。慢性心不全におけるリハビリテーションには骨格筋萎縮やエルゴリフレックスの亢進など取り組むべき問題は多く、このような全人的アプローチが今後の心不全治療には必須と考えられます。心不全患者における心臓リハビリテーションや心身医学を科学的に評価し、臨床応用に繋がるよう取り組んでいます。 -
心血管カテーテル治療分門
当科のカテーテル検査室では、豊富な症例数と最新の治療機器を用いた臨床研究に加え、関連病院を含めた多施設共同研究の主導やそのデータを用いた学会発表、ならびに論文作成を行っています。PCI治療抵抗性重症患者(糖尿病、透析、高齢者等)や心房細動合併症例に対するPCI後の予後に関する研究や、重症下肢虚血を含めた閉塞性動脈硬化症の治療成績に関する検討等数多くの実績を挙げています。
国内・海外を含めた共同治験、登録研究や、国内未承認デバイスの治験などにも積極的に参加しており、近年では重症僧房弁閉鎖不全症に対するカテーテル治療(MitraClip®)の治験施設にも選定されています。Impact of visit-to-visit variability and systolic blood pressure control on subsequent outcomes in hypertensive patients with coronary artery disease (from the HIJ-CREATE substudy).
Arashi H, Ogawa H, Yamaguchi J, Kawada-Watanabe E, Hagiwara N.
Am J Cardiol. 2015 Jul 15;116(2):236-42. doi: 10.1016/j.amjcard.2015.04.011. Epub 2015 Apr 20.Impact of left ventricular ejection function on blood pressure-lowering therapy in hypertensive patients with coronary artery disease.
Kikuchi N, Jujo K, Yamaguchi J, Ogawa H, Hagiwara N.
J Hypertens. 2016 May;34(5):1011-8. doi: 10.1097/HJH.0000000000000874.Effect of Hemodialysis on 7-Year Clinical Outcomes After Sirolimus-Eluting Stent Implantation.
Buronova N, Kamishima K, Yamaguchi J, Jujo K, Watanabe E, Inagaki Y, Kishi S, Wada A, Hatakeyama S, Watanabe M, Nakao M, Okayama D, Arashi H, Yamada N, Takagi A, Ogawa H, Hagiwara N.
Circ J. 2015;79(10):2169-76. doi: 10.1253/circj.CJ-15-0113. Epub 2015 Aug 25.A randomized trial evaluating everolimus-eluting Absorb bioresorbable scaffolds vs. everolimus-eluting metallic stents in patients with coronary artery disease: ABSORB Japan.
Kimura T, Kozuma K, Tanabe K, Nakamura S, Yamane M, Muramatsu T, Saito S, Yajima J, Hagiwara N, Mitsudo K, Popma JJ, Serruys PW, Onuma Y, Ying S, Cao S, Staehr P, Cheong WF, Kusano H, Stone GW; ABSORB Japan Investigators.
Eur Heart J. 2015 Dec 14;36(47):3332-42. doi: 10.1093/eurheartj/ehv435. Epub 2015 Sep 1. Review.Real clinical practice of catheter therapy for deep venous thrombosis: periprocedural and 6-month outcomes from the EDO registry.
Mizuno A, Anzai H, Utsunomiya M, Yajima J, Ohta H, Ando H, Umemoto T, Higashitani M, Ozaki S, Sakamoto H, Nakao M, Yuzawa Y, Kaneko H, Nakamura M; EDO registry investigators.
Cardiovasc Interv Ther. 2015 Jul;30(3):251-9. doi: 10.1007/s12928-014-0314-0. Epub 2015 Jan 10.Effect of concurrent elevation of serum creatinine and C-reactive protein values on the long-term outcome in patients with ST-elevation acute myocardial infarction.
Kamishima K, Yamaguchi J, Honda A, Ogawa H, Hagiwara N.
Int J Cardiol. 2015 Jun 1;188:102-4. doi: 10.1016/j.ijcard.2015.04.048. Epub 2015 Apr 8. No abstract available.Percutaneous coronary intervention for left main compression syndrome due to severe idiopathic pulmonary arterial hypertension: one year follow-up using intravascular imaging.
Ogiso M, Serizawa N, Kamishima K, Yamaguchi J, Hagiwara N.
Intern Med. 2015;54(7):801-4. doi: 10.2169/internalmedicine.54.3528. Epub 2015 Apr 1.Effects of Statin versus the Combination of Ezetimibe plus Statin on Serum Lipid Absorption Markers in Patients with Acute Coronary Syndrome.
Watanabe E, Yamaguchi J, Arashi H, Ogawa H, Hagiwara N.
J Lipids. 2015;2015:109158. doi: 10.1155/2015/109158. Epub 2015 Mar 1.Three-Year Clinical Outcomes of Everolimus-Eluting Stents From the Post-Marketing Surveillance Study of Cobalt-Chromium Everolimus-Eluting Stent (XIENCE V/PROMUS) in Japan.
Aoki J, Kozuma K, Awata M, Nanasato M, Shiode N, Tanabe K, Yamaguchi J, Kusano H, Nie H, Kimura T; XIEVCE V/PROMUS PMS Investigators.
Circ J. 2016 Mar 25;80(4):906-12. doi: 10.1253/circj.CJ-15-1181. Epub 2016 Jan 27.Prognostic impact of spontaneous coronary artery dissection in young female patients with acute myocardial infarction: A report from the Angina Pectoris-Myocardial Infarction Multicenter Investigators in Japan.
Nakashima T, Noguchi T, Haruta S, Yamamoto Y, Oshima S, Nakao K, Taniguchi Y, Yamaguchi J, Tsuchihashi K, Seki A, Kawasaki T, Uchida T, Omura N, Kikuchi M, Kimura K, Ogawa H, Miyazaki S, Yasuda S.
Int J Cardiol. 2016 Mar 15;207:341-8. doi: 10.1016/j.ijcard.2016.01.188. Epub 2016 Jan 14. - Adult congenital
- 心エコー
- 心臓リハビリテーション
- 心臓放射線
- 大規模臨床研究
カテーテルアブレーション
植え込み型デバイス
そこでの臨床データを活用し、HIJC(The Heart Institute of Japan, Cardiology)研究グループとして多施設共同研究を実施し、日本における心臓病のエビデンスを確立することを目指してきました。日本人の急性心筋梗塞の予後を明らかにするために1999年に登録を開始したHIJAMI研究を皮切りに、これまで数多くの観察研究・介入試験を行ってきました。その成果は循環器内科医局員の全てが共有し、下に示す通り国内外の一流誌に掲載されてきました。
現在、脂質異常症を合併した急性冠症候群を対象とした前向き介入試験(HIJ-PROPER)を実施しており、2016年夏にその成果を公開することを目標に最終段段階に差し掛かっています。ここからも数多くのエビデンスを生みだすことが期待できます。 そのためにも臨床・研究に、ともに取り組んでくれる若い力が必要です。
日本全国から夢に溢れた将来の循環器専門医が、多数仲間に入ってくれることを期待しています。
【HIJC研究グループの成果】
J Hypertens. 2016 May;34(5):1011-8.
Am J Cardiol. 2015 Jul 15;116(2):236-42.
Int J Cardiol. 2015 Jun 1;188:102-4.
J Lipids. 2015;2015:109158.
J Cardiol. 2013 Oct;62(4):217-23.
Int J Cardiol. 2013 Sep 10;167(6):2490-5.
Am J Cardiol. 2012 Feb 15;109(4):576-80.
Int J Cardiol. 2012 Sep 6;159(3):205-10.
Am J Cardiol. 2010 Sep 15;106(6):819-24.
Blood Press. 2010 Dec;19(6):359-65.
Cardiovasc Diabetol. 2010 Jan 4;9:1.
Eur Heart J. 2009 May;30(10):1203-12.
Circ J. 2008 Dec;72(12):2015-20.
Heart. 2009 Mar;95(3):216-20.
Circ J. 2008 Sep;72(9):1391-6.
Cardiovasc Drugs Ther. 2008 Jun;22(3):177-84.
Circ J. 2008 Feb;72(2):179-85.
Circ J. 2007 Sep;71(9):1354-9.
Am J Cardiol. 2007 Jun 1;99(11):1523-8.
Am Heart J. 2005 Sep;150(3):411-8.
Am J Cardiol. 2004 Jun 15;93(12):1526-8.
基礎
- 血栓・凝固
- 動脈硬化
- 再生医療
- 病理
臨床
動脈硬化疾患・原発性脂質異常症
原発性脂質異常症のうち家族性高コレステロール血症(FH)、 家族性III型高脂血症、高カイロミクロン血症(高CM血症)は心血管疾患合併の多い脂質異常症で、FHと高CM血症は指定難病に認定されています。
FHは常染色体性優性遺伝型式を示す遺伝子異常で、ホモ接合体は100万人に1人と稀ですが、FHヘテロ接合体は200-500人に1人と高頻度で見られます。FHホモ接合体、ヘテロ接合体ともに、幼少期より高コレステロール血症を示し、若年性動脈硬化症による心筋梗塞などの重篤な病気を引き起こすため、できるだけ早期に診断を下し、積極的に血清コレステロール値を低下する治療を開始することが重要です。FHヘテロ接合体は若年発症の冠動脈疾患患者の10-20人に1人いると推測されていますが、日本での診断率は1%未満と診断率の高い北欧諸国から大きく遅れをとっています。当教室では、急性冠症候群をはじめとする心血管疾患におけるFH患者の診断と加療および動脈硬化の評価、また罹患率と予後の解析を行っています。高コレステロール血症、アキレス腱の肥厚、家族歴などの情報のみでは診断が困難な例や重症例には、FHの確定診断の決め手となるLDL受容体の遺伝子診断、類似疾患である家族性欠陥アポリポ蛋白B-100(FDB)症、常染色体劣性遺伝性高コレステロール血症(ARH)、アポリポ蛋白E異常症、Proprotein convertase subtilisin kexin 9(PCSK9)などの遺伝子変異、また高CM血症についても遺伝子変異を解析し、希望された患者には遺伝子カウンセリングを行っています。
基礎
動脈硬化・心臓免疫炎症
急性冠症候群(ACS)、虚血性心疾患による心不全は致死率の高い疾患です。また、慢性腎臓病は心血管イベント増加に関連しています。そのため、動脈硬化の進展、ACSを発症する冠動脈の粥腫不安定化機序、動脈硬化による慢性腎臓病、心不全の免疫学的病態を解明することは非常に重要です。動脈硬化進展や粥腫不安定化には慢性炎症やT細胞サブセットによる獲得免疫、血管壁に発現する接着分子が深くかかわっています。当研究室では科学研究費などの公的助成金を得て、ACS、更年期女性、心不全患者の血中サイトカイン、末梢単核球やCD4 T細胞、冠動脈や心筋組織を解析しています。さらに、その結果を動脈硬化モデルマウスなどの遺伝子改変マウスの血管や心臓、腎臓で検証し、薬剤の効果や新しい治療の検討を行っています。研究成果は、積極的に国際学会をはじめとする多数の学会や論文で発表し、学会賞など多数受賞しています。
1)ヒト心筋組織の分子生物学的および機能的解析を踏まえた効果的な心筋再生医療の創出
2)遺伝性心疾患iPS細胞技術との融合による生体外でのヒト心筋組織機能解析を通した疾患・創薬研究
3)心臓間質細胞の分子生物学的特性修飾による血管新生
を通して新たな心不全治療の開発を行っています。
1) ヒトiPS細胞由来心筋組織による心筋再生研究
現在国内外で生体由来細胞を用いた再生医療が虚血・非虚血性心不全を対象に行われています。しかし現行の心臓再生医療は、移植細胞の分泌する増殖因子などによる心筋保護・血管新生効果によるものであり、障害により低下した心機能に伴う心拍出量の低下を心筋組織の補填により直接的に補うものではありません。また、世界的には、その簡便さから細胞単体を心臓へ直接移植したり、経冠動脈的に移植する手法が一般的ですが、このような移植法では、その多くが移植後に生着しないことが分かっています。一方で、生体外で細胞を組織状に加工し移植することで、より多くの細胞が生着し、心機能向上に寄与することが明らかとなっています。東京女子医大では、日本発世界初の細胞シート技術により生体外で組織を構築することが可能です。また最近では、同じく東京女子医大独自のヒトiPS細胞大量培養技術により、ヒト心筋細胞、血管内皮細胞および間質細胞の量産が可能となり、細胞シート技術により作成したヒト心筋組織を用いた研究開発が日常的に行なわれています。
このようにヒト心筋組織を用いることで、不全心による心拍出量の低下を直接的に補う新たな心不全治療の開発が可能と考えますが、その臨床応用に向けては解決すべき課題がまだ数多く存在します。
一つは、心筋の成熟化です。iPS細胞より分化した心筋細胞は胎児期の心筋細胞と同等と考えられ、成体の作業心筋程度にまで成熟化を図ることが重要です。心筋細胞の成熟化に関する研究は、再生医療への応用はもちろんですが、胎児期から成体に至るまでの心筋細胞の成熟過程を分子生物学的に理解することとなり、我々が普段の日常診療の中で扱っている心筋細胞自体への理解が深まるものと考えます。
二つ目は、心不全モデル動物への心筋組織移植による心機能改善およびその機序の解明です。虚血・非虚血性心疾患における左心不全とともに、先天性心疾患による右心不全も心筋再生医療が貢献できる対象と考えています。十分な機能を示すための再生心筋組織の厚みや血管網、代謝などを最適化し、小動物から大動物に至るまで最適な疾患モデル動物を用いて心拍出量の補助としての効果を検証することが必要です。
三つ目は、iPS細胞を含む多能性幹細胞を用いる上でのリスク軽減です。多能性幹細胞は無限増殖能と多分化能を有しているため、移植心筋組織内に未分化細胞が残存すると、移植後に腫瘍を形成するリスクが高くなります。特に心筋再生医療においては、移植する細胞数が大変多いため、未分化細胞が残存するリスクも相対的に高いものになりますので、様々な機序をベースとした複数の残存未分化細胞除去の手法を用いることが必要です。心筋細胞などの分化細胞とヒトiPS細胞との間の、代謝や細胞増殖シグナルそしてストレスに対する反応性などの相違を指標に、未分化細胞除去手法の開発を行っています。
これらの3つの課題以外にも、再生心筋組織を用いた再生医療の適応の幅を広げていく中で出てくる課題を解決し、一日も早く重症心不全に対する効果的な心筋再生医療を開発します。
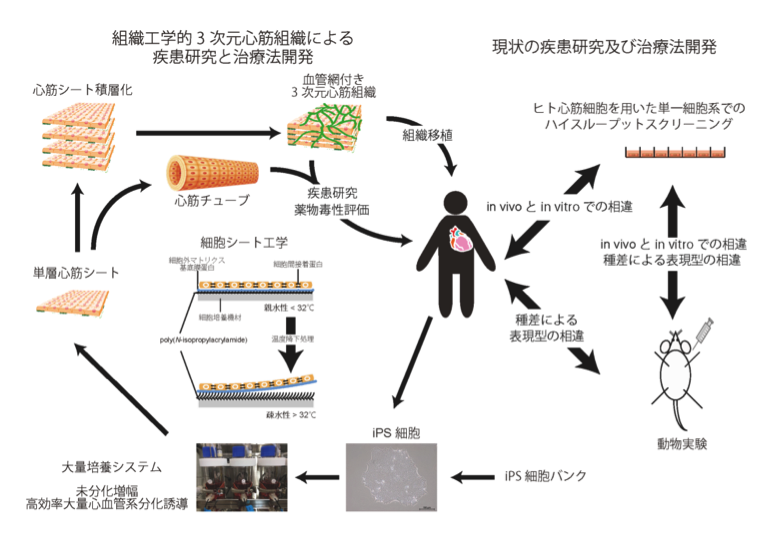
2) ヒト心筋組織技術と疾患iPS細胞による疾患・創薬研究
ヒト心筋組織は、再生医療への応用のみならず、疾患・創薬研究への応用も可能です。疾患・創薬研究において、遺伝子組み換え動物や疾患モデル動物を用いた検討は現在でも標準的に行なわれていますが、ヒトと動物間の種差による疾患表現型や薬物への応答性の相違が、動物での結果をヒトへ応用する際の大きなハードルとなっています。また細胞レベルでの解析は、スループット性に優れている一方で、生体は組織内細胞が相互に影響し合い機能を保持している点で細胞レベルでの解析の限界も存在します。したがって、生体外でのヒト心筋組織を用いた機能解析およびその各種病態を模擬した培養環境における分子生物学的な解析は、ヒトの心臓の病態に関する新たな知見を創出することが期待され、また創薬研究などへの応用においても組織レベルでの機能への効果を検証できる点で、大変有用と考えます。さらに近年発展著しい疾患iPS細胞技術と融合させることで、疾患心筋組織を構築することも可能です。ゲノムに由来する心疾患を組織レベルで機能とともに解析し、さらにゲノム編集技術を駆使することで機能異常の原因遺伝子を確定することにもつながります。
この研究開発の発展により、各種疾患へのより早期からの効果的な介入が可能となることで、心不全の発症を抑制することが目標となります。
3) 心臓間質細胞機能制御による心不全治療法開発
普段我々は、生まれ成熟して出来上がった心臓、そして各種疾患によって障害を受けた心臓を診ることで、病態を理解し治療に繋げています。一方、組織工学を用いて心筋組織を構築するには、心筋細胞や血管、間質細胞を含む構成細胞の特性および相互作用を理解しつつ、それらを適切に組み合わせることが必要です。したがって、心筋組織を構築する中で観察される各細胞同士の組み合わせによる様々な現象やその分子機序は、我々の心臓においても生じている現象と考えられ、延いては我々の心臓自体をより良く理解することに繋がります。心臓は、体積としては心筋細胞が大半を占めますが、細胞数としては間質の細胞が約7割程度を占めると言われています。さらに心筋梗塞などの障害後の心筋組織は、多くが線維性組織に置換されることからも、間質細胞の特性の理解が治療ターゲットになることが予想されます。最近我々は、心臓由来間質細胞が、他の臓器の間質細胞とは異なり、心筋細胞や血管の細胞に対して特異的な機能を有することを見出し、そのベースにある心臓間質細胞の分子生物学的な特性を明らかにしつつあります。生体の心臓に数多く存在する間質細胞のこのような機能への介入手法を開発することで、心筋細胞死抑制や血管新生促進を介した虚血性心疾患および心不全に対する新規治療法を創出できるものと考えます。
東京女子医科大学 循環器内科 医局長 春木 伸太郎
| TEL | 03-3353-8111(内線23110) |
|---|---|
| FAX | 03-3356-0441 |
| meditop.au@twmu.ac.jp | |
| 所在地 | 東京都新宿区河田町8-1 |
見学、ご相談は随時行っております。当科での後期臨床研修を考えておられる先生方は是非ご連絡ください。










